- » Антропология
- » Археология
- » Архитектура
- » Астрономия
- » Библиотековедение
- » Биология
- » Биотехнологии
- » Ботаника
- » Ветеринария
- » Военные науки
- » География
- » Геология
- » Журналистика
- » За горизонтом современной науки
- » Зоология
- » Информационные технологии
- » Искусствоведение
- » История
- » Культурология
- » Лингвистика
- » Литература
- » Маркетинг
- » Математика
- » Машиностроение
- » Медицина
- » Менеджмент
- » Методика преподавания
- » Музыковедение
- » Нанотехнологии
- » Науки о Земле
- » Образование
- » Оптика
- » Педагогика
- » Политология
- » Правоведение
- » Психология
- » Регионоведение
- » Религиоведение
- » Сельское хозяйство
- » Социология
- » Спорт
- » Строительство
- » Телекоммуникации
- » Техника
- » Туризм
- » Управление и организация
- » Управление инновациями
- » Фармацевтика
- » Физика
- » Физическая культура
- » Филология
- » Философия
- » Химия
- » Экология
- » Экономика
- » Электроника
- » Электротехника
- » Юриспруденция
УРАВНЕНИЕ СОСТОЯНИЯ ПРОДУКТОВ ДЕТОНАЦИИ ОКТОГЕНА ИЗ ЭКСПЕРИМЕНТА И ИЗ ТЕРМОХИМИЧЕСКОГО РАСЧЕТА
Изучение кинетики реакции восстановления гексацианоферрата калия (II) и гексацианоферрата калия (III) аскорбиновой кислотой
АНАЛИЗ УРАВНЕНИЯ СОСТОЯНИЯ ПРОДУКТОВ ДЕТОНАЦИИ TKX-50, ПОЛУЧЕННОГО В ТЕРМОХИМИЧЕСКОМ РАСЧЕТЕ
Оценка влияния содержания лигнина в фенолформальдегидной смоле на огнестойкость фенольной пены
Разделы: Нанотехнологии, Техника, Химия
Размещена 12.08.2014. Последняя правка: 11.08.2014.
Просмотров - 5058
МЕХАНИЗМ ФОРМИРОВАНИЯ И КОРРОЗИОННОЕ ПОВЕДЕНИЕ НАНОСТРУКТУРИРОВАННЫХ ОКСИДНЫХ ПОКРЫТИЙ НА НИОБИИ
Токарева Ирина Анатольевна
НТУ "ХПИ"
аспирант
Научный руководитель: Байрачный Борис Иванович, доктор технических наук, профессор каф. технической электрохимии Национального технического университета «Харьковский политехнический институт»
УДК 621.35
Введение
Ниобий и его сплавы применяют в различных отраслях современной промышленности. Высокое сродство к кислороду обуславливает наличие на поверхности ниобия естественной пассивирующей оксидной пленки, которая защищает металл от химического воздействия, повышая его коррозионную стойкость.
Одним из методов, позволяющих улучшить эксплуатационные характеристики ниобия и расширить области его применения, является метод анодного окисления, приводящий к образованию на металлической поверхности оксидной пленки, которая в зависимости от условий получения может иметь различные свойства. Состав электролита и режим анодирования позволяют контролируемо варьировать основные параметры формируемого анодного оксидного покрытия (АОП) [1, 2].
Анализ опубликованных работ [3–5] показывает, что при анодировании ниобия во фторидсодержащих электролитах на его поверхности образуется наноструктурированное оксидное покрытие. Проведенные на сегодня исследования АОП ниобия в основном посвящены установлению корреляции между параметрами технологического процесса, составом электролитов и морфологическими особенностями синтезируемого оксидного слоя. Однако до сих пор нет ясности в вопросах механизма формирования пористого АОП на ниобии, нет единой кинетики роста оксида, неясна роль окисляющей среды и влияния электрофизических факторов.
В последние годы появились данные по использованию наноструктурированных АОП ниобия. Так, например, пористые пленки Nb2O5 считаются перспективным электродным материалом, который можно применять для увеличения эффективности сенсибилизированных красителем солнечных элементов (батарей) [6]. В работе [7] показана возможность использования пористой анодной пленки оксида ниобия в качестве катода для литий-ионных аккумуляторов. Кроме того, известно, что оксид ниобия имеет хорошую биологическую совместимость и является потенциальным кандидатом для модификации поверхности металлических имплантатов [8, 9]. Широкое внедрение в практику этого материала сдерживается, прежде всего, из-за отсутствия комплексных материаловедческих исследований. В связи с этим, в данной работе рассмотрен механизм формирования и проведена оценка коррозионной стойкости наноструктурированных АОП, синтезированных на ниобии при анодной поляризации во фторидсодержащих электролитах.
Экспериментальная часть
В качестве исходного материала рабочих электродов использовали ниобиевую фольгу толщиной 0,1 мм, чистотой 99,99 %. Подготовка рабочей поверхности ниобия включала химическое полирование образцов в смеси концентрированных кислот с объемным соотношением H2SO4 : HNO3 : HF = 5 : 2 : 2 в течение 5 – 10 с.
Формирование АОП на ниобии проводили по двухэлектродной схеме в электролитической ячейке из фторопласта. Процесс анодирования осуществляли в вольтстатическом режиме при комнатной температуре с использованием стабилизированного источника постоянного тока серии Б5-50. Величину напряжения и тока в системе контролировали с помощью цифровых универсальных вольтметров В7-35. Условия электросинтеза АОП приведены в табл. 1.Таблица 1 – условия анодирования ниобия
|
№ покрытия |
Состав раствора |
Напряжение, В |
Время, ч |
|
1 |
1 М H2SO4 + 0,25 М HF |
20 |
1 |
|
2 |
1 М H2SO4 + 0,5 М NаF |
60 |
2 |
Морфологию поверхности синтезированных образцов исследовали методом сканирующей электронной микроскопии (СЭМ) на микроскопе JSM-7001F. Рентгенофазовый анализ пленок осуществляли на дифрактометре ДРОН-2 (СuKα-излучение).
Коррозионные испытания покрытий проводили в растворах: 0,1 М H2SO4; 0,15 М NaCl; 0,1 М NaOH. Скорость коррозии определяли по результатам анализа анодных и катодных поляризационных зависимостей полученных на потенциостате ПИ-50-1.1 в потенциостатическом режиме. Экстраполяцией прямолинейных участков анодной либо катодной поляризационной кривой на стационарный потенциал определяли плотность тока коррозии (jкор, А/м2) и рассчитывали ее скорость (К, г/м2ч) по формуле [10]: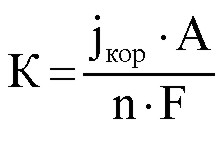
где А – атомная масса оксида;
n – валентность ионов металла;
F – постоянная Фарадея.
Обсуждение результатов
Воздействие условий обработки на свойства АОП является непростой темой, так как большинство переменных, которые необходимо при этом учитывать, являются взаимосвязанными. Анализируя полученные экспериментальные результаты можем утверждать, что при анодном окислении ниобия во фторидсодержащих растворах, на металле формируется наноструктурированное оксидное покрытие, морфологические особенности которого задаются составом электролита и режимом электролиза.
При взаимодействии аниона активатора (F–) c поверхностными атомами металла могут образовываться промежуточные комплексы, которые переходят в раствор и гидролизуются [11]. Химическое взаимодействие фторидсодержащего электролита с поверхностью оксидного слоя ниобия может быть описано реакциями [12]:
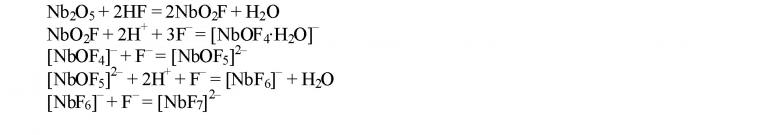
На основании проведенных исследований и анализа литературы механизм анодной активации ионами фтора АОП ниобия можно представить следующим образом. Центрами зарождения процесса активации являются слабые дефектные места оксидной пленки, которые характеризуются повышенной электронной проводимостью по сравнению с остальной поверхностью анода. При достаточно высоком анодном потенциале падение потенциала на этой части межфазной границы может достичь величины, при которой происходит адсорбционное вытеснение ионами фтора с поверхности оксида частиц, содержащих кислород и необходимых для образования (роста) оксидной пленки. Разрушающее действие фтора на АОП связывают с его высокой проникающей способностью.
Адсорбция активирующих анионов с вытеснением частиц, содержащих кислород, приводит к тому, что на дефектных местах процесс образования (роста) АОП затрудняется, а при высокой концентрации F– и вовсе прекращается. Вместо этого происходит образование растворимых в воде соединений ниобия с фтором. Взаимодействие образовавшихся фторидных соединений ниобия с водой приводит к удалению продуктов реакции с анода. При определенной концентрации F– в электролите анодирования ниобия, происходит локальное растворение оксидной пленки, способствующее формированию пористого оксидного слоя (рис. 1). Под действием сильного электрического поля происходит кристаллизация оксида, приводящая к формированию кристаллического АОП, имеющего развитую наноструктурированную морфологию.
Микрофотографии поверхности АОП синтезированных в данной работе, приведены на рис. 1. Методом рентгенофазового анализа установлено, что покрытие № 1 (рис. 1 а) является рентгеноаморфным, а покрытие № 2 (рис. 1 б) имеет кристаллическую структуру. Кроме того, толщина аморфной пленки составляет около 160 нм, а кристаллической 3 мкм. Очевидно, что подобные особенности в морфологии и структуре покрытий существенно скажутся на их свойствах, в частности коррозионной стойкости АОП в различных средах. 

|
Рис. 1. – СЭМ поверхности анодного оксида ниобия: а) покрытие № 1; б) покрытие № 2. |
Результаты коррозионных испытаний (рис. 2) подтверждают предположения о различии в свойствах, сформированных на ниобии АОП. Основные характеристики коррозионного поведения исследуемых покрытий приведены в таблицах 2 и 3. Несмотря на различие значений потенциалов коррозии аморфных и кристаллических пленок, наблюдается аналогия в их изменении. При переходе от кислой среды к нейтральной и щелочной потенциал коррозии смещается в более электроотрицательную область. Коррозионная стойкость кристаллических покрытий ниобия на порядок выше аморфных АОП. Скорее всего, это связано с толщиной оксида.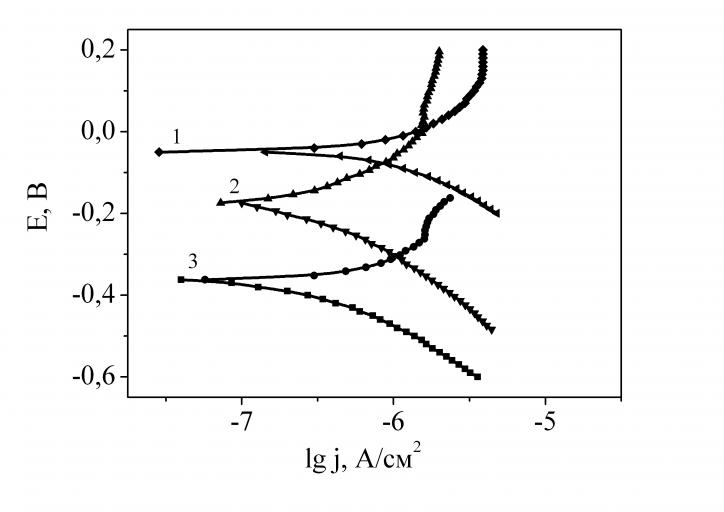
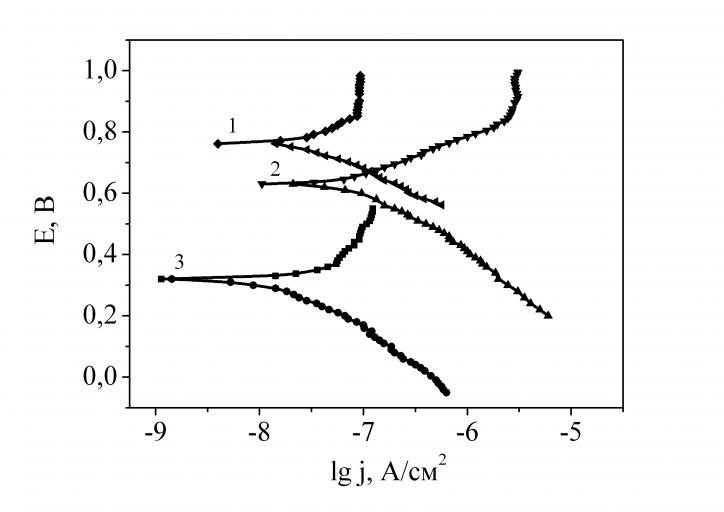
Рис. 2 – поляризационные зависимости, полученные на аморфных (а) и кристаллических (б) АОП ниобия в растворах: 1) 0,1 М H2SO4; 2) 0,15 М NaCl; 3) 0,1 М NaOH.
Таблица 2 – Показатели коррозии аморфного АОП ниобия (покрытие № 1)
|
Среда |
Показатель коррозии |
||
|
Екор, В |
lg jкор, А/cм2 |
К, г/м2ч |
|
|
0,1 М H2SO4 |
– 0,05 |
– 6,21 |
3,4·10–10 |
|
0,15 М NaCl |
– 0,174 |
– 6,46 |
1,91·10–10 |
|
0,1 М NaOH |
– 0,36 |
– 6,39 |
2,25·10–10 |
Таблица 3 – Показатели коррозии кристаллического АОП ниобия (покрытие № 2)
|
Среда |
Показатель коррозии |
||
|
Екор, В |
lg jкор, А/cм2 |
К, г/м2ч |
|
|
0,1 М H2SO4 |
0,52 |
– 7,75 |
9,8·10–12 |
|
0,15 М NaCl |
0,18 |
– 7,19 |
3,56·10–11 |
|
0,1 М NaOH |
0,02 |
– 7,96 |
6,04·10–12 |
Выводы
Таким образом, при формировании АОП на ниобии ключевыми факторами, определяющими свойства оксидного слоя являются концентрация активатора (фторид-ионов) и напряжение анодирования. Наноструктурированные АОП на ниобии демонстрируют высокую коррозионную стойкость, что позволяет рекомендовать их для практического использования в различных агрессивных средах.
1. Байрачный Б.И., Андрющенко Ф.К. Электрохимия вентильных металлов Х: «Вища школа», Издательство при Харьковском университете, 1985. – 144 с.
2. Одынец Л.Л. Анодные оксидные пленки – Ленинград: Наука, 1990. – 200 с.
3. Kim Н.K., Yoo J.E., Park J. et al. Formation of niobium oxide film with duplex layers by // Bull. Korean Chem. Soc. – 2012. – V. 33. – № 8. – рр. 2675 – 2678.
4. Sieber I., Hildebrand H., Friedrich A., Schmuki P. Formation of self-organized niobium porous oxide on niobium // Electrochemistry Communications. – 2005. – V. 7, № 1. – pp. 97 – 100.
5. Oikawa Y., Minami T., Mayama H., Tsujii K. Preparation of self-organized porous anodic niobium oxide microcones and their surface wettability // Acta Materialia. – 2009. – V. 57. – рр. 3941 – 3946.
6. Ou J.Z., Rani R.A., Ham M.H. Elevated temperature anodized Nb2O5: a photoanode material with exceptionally large photoconversion efficiencies // Acsnano. – 2012. – Vol. 6, № 5. – рр. 4045 – 4053.
7. Yoo J.E., Park J., Cha G. Micro-length anodic porous niobium oxide for lithium-ion thin film battery applications // Thin Solid Films. – 2013. – V. 531. – pp. 402 – 751.
8. Eisenbarth E., Velten D., Muller M. et al. Nanostructured niobium oxide coatings influence osteoblast adhesion // Journal of Biomedical Materials Research. – 2006. – V. 79A. – рр. 166 – 175.
9. Pauline S.A., Rajendran N. Biomimetic novel nanoporous niobium oxide coating for orthopaedic applications // Applied Surface Science. – 2014. – V. 290. – рр. 448 – 457.
10. Куделин Ю.И., Легезин Н.Е. Методические указания по испытанию ингибиторов коррозии для газовой промышленности. – ВНИИГАЗ, 1996 – 48 с.
11. Камкин А.Н. Закономерности анодно-анионной активации ниобия: автореф. дис. на соискание уч. степени канд. хим. наук: спец. 02.00.05 «Электрохимия» – Москва, 1981. – 20 с.
12. Lu H., Gautier R., Donakowski M.D. et al. From solution to the solid state: control of niobium oxide−fluoride [NbOxFy]n− species // Inorganic Chemistry. – 2014. – V. 53. – pp. 537 – 542.
Рецензии:
12.08.2014, 12:24 Каменев Александр Юрьевич
Рецензия: Неплохой материал экспериментальных исследований, обладающий актуальностью и элементами научной новизны. Следует только переименовать раздел "Обсуждение результатов" в "Анализ результатов" или "Обработка результатов", т.к. обсуждение предполагает некую публичную дискуссию, а не работу автора. Рекомендуется к печати.
23.08.2014, 17:52 Назарова Ольга Петровна
Рецензия: Смущает проведение эксперимента с "взаимосвязанными" факторами?! Хотелось бы порекомендовать в качестве методики ПФЭ. В целом материал интересный. Рекомендуется к печати
3.09.2014, 19:11 Мухуров Николай Иванович
Рецензия: Актуальность работы не вызывает сомнений. Статья содержит все требуемые элементы: цель, задачи, методика, используемые оборудование и методы анализа. Иллюстративный материал достаточен для обсуждения полученных результатов и сделанных выводов. Возможно дополнить выводы еще одним-двумя предложениями. Следует обратить внимание автора на расстановку запятых в тексте. Рекомендуется к печати.
Комментарии пользователей:
Оставить комментарий
Вверх