- » Антропология
- » Археология
- » Архитектура
- » Астрономия
- » Библиотековедение
- » Биология
- » Биотехнологии
- » Ботаника
- » Ветеринария
- » Военные науки
- » География
- » Геология
- » Журналистика
- » За горизонтом современной науки
- » Зоология
- » Информационные технологии
- » Искусствоведение
- » История
- » Культурология
- » Лингвистика
- » Литература
- » Маркетинг
- » Математика
- » Машиностроение
- » Медицина
- » Менеджмент
- » Методика преподавания
- » Музыковедение
- » Нанотехнологии
- » Науки о Земле
- » Образование
- » Оптика
- » Педагогика
- » Политология
- » Правоведение
- » Психология
- » Регионоведение
- » Религиоведение
- » Сельское хозяйство
- » Социология
- » Спорт
- » Строительство
- » Телекоммуникации
- » Техника
- » Туризм
- » Управление и организация
- » Управление инновациями
- » Фармацевтика
- » Физика
- » Физическая культура
- » Филология
- » Философия
- » Химия
- » Экология
- » Экономика
- » Электроника
- » Электротехника
- » Юриспруденция
Разделы: Медицина
Размещена 20.06.2014. Последняя правка: 20.06.2014.
Просмотров - 7575
ПРОКАРИОТ-ГЕНЕТИЧЕСКАЯ ЭПИГЕНЕTИЧЕСКАЯ ТЕОРИЯ КАНЦЕРОГЕНЕЗА, АССОЦИИРОВАННОГО С HELICOBACTER PYLORI
Кованова Эльвира Николаевнаканд.мед.наук, доцент
Тернопольский медуниверситет
доцент кафедры
Климнюк Сергей Иванович, профессор, заведующий кафедрой Тернопольского государственного медуниверситета, e-mail klymnyuk@yahoo.com Творко Михаил Стефанович, доцент, доцент кафедры Тернопольского государственного медуниверситета, e-mail tvorko@ukr.net
УДК 576.385.5\.579.835.12
Прокариот Helicobacter pylori - первый и пока единственный микроорганизм, у которого удалось установить связь с онкогенезом человека. Многочисленные факторы патогенности Helicobacter pylori - продукты генов cagA и vacA,- помогают расскрывать механизм провоспалительных реакций при неонкогенных хеликобактериозах: остром, хроническом, атрофическом гастрите, язвенной болезни. Однако до сих пор считаются неизвестными механизмы малигнизации, в том числе и молекулярные, acсоциированные с бактерией при дистальной аденокарциноме желудка и MALT лимфоме.
В то же время в результате экспериментальных исследований последних десятилетий, проведенных in vitro и in vivo, в геноме Helicobacter pylori обнаружены генетические элементы непосредственно связанные с онкогенезом, такие как онкогены бактерии cagA, vacA, babA2 [11 с.2], новый регион i1 гена vacA [12 с.2]. Главный фактор патогенности при провоспалительных хеликобактериозах. Экспериментами, проведенными на молекулярном уровне, удалось установить особенности тирозинкиназного фосфорилирования продуктов онкогенов Helicobacter pylori, непосредственно связанных с канцерогенезом.agA оказался первым онкобелком бактериального происхождения, вовлеченным в карциногенез [4 с.2; 5 с.2; 5,10 с.2].
Эти и другие исследования по этому вопросу дают возможность проследить связь генетического онкогенного потенциала бактерий с патогенезом заболеваний и, прежде всего, сделать заключение о соответствии онкогенеза бактерии общим механизмам туморогенеза: онкоген → онкобелок → трансформация → туморогенез, как это представлено для хеликобактера на табл. 1
|
Helicobacter pylori |
|||
|
Онкогены |
Протеины |
→ |
Дистальная аденокарцинома желудка, MALT лимфома |
|
cagA |
онкопротеин CagA |
||
|
vacA |
протеин VacA |
||
|
babA2 |
протеин BabA2 |
||
Табл. 1. Схема онкогенеза Helicobacter pylori
До сих пор считается, что только онкогены вирусов обладают канцерогенными свойствами, а для прокариотов аналогичная канцерогенная активность остается не установленной. При онкогенных хеликобактериозах канцерогенез ассоциируют с генотоксическими веществами, свободными радикалами, перекисью водорода вблизи Helicobacter pylori [2 c.2].
В то же время результаты экспериментальных исследований показывают, что триггерами хеликобактерного канцерогенеза, как и вирусного, являются онкогены бактерии. Прокариот-генетический путь, как оказалось, имеет более сложный механизм по сравнению с вирусами, так как вирулентные штаммы Helicobacter pylori кроме онкогенного потенциала хеликобактерии вовлекают в канцерогенез также рецептор эпидермального фактора роста (EGFR).
Прокариот-генетический путь канцерогенеза хеликобактера, детерминируемый онкогенами бактерии cagA, vacA, babA2, во многом соответствует вирусо-генетической теории Л.А. Зильбера. Вирусный канцерогенез ретровирусов животных также как и прокариотный контролируется онкогенами по подобному механизму. Аналогичное онкогенное детерминирование х - онкогеном обнаружено в последнее время и у ДНК вируса гепатита В [7 с.3]. Главным в механизме хеликобактерного канцерогенеза, как и для вирусного, является тирозинкиназное фосфорилирование, нехарактерное для нормального метаболизма клеток.
Подобно низкоонкогенным медленнодействующим онкорнавирусам Helicobacter pylori индуцирует канцерогенез после длительного (10-15 лет) латетного периода.
В то же время бактериальный онкогенез имеет и некоторые особенности, которые отличают его от вирусного.
Как правило, при вирусном канцерогенезе за онкогенез отвечают отдельные гены - онкогены, которые не несут иных функций кроме канцерогенеза. У бактерии за канцерогенез отвечают три онкогена бактерии - cagA, vacA, babA2, локализованные в хромосоме и острове патогенности cag PAI. Ранее они рассматривались только как гены, контролирующие факторы патогенности. Как было установлено, ген cagA - главный ген патогенности Helicobacter pylori локализованный в острове патогенности cag PAI около 60 % штаммов, отвечает за воспаление. Ген vacA, присутствующий в хромосоме 100 % штаммов, детерминирует продукцию вакуолизирующего цитотоксина. Ген babA2 отвечает за адгезию бактерий.
Основанием для оценки генов cagA, vacA, babA2, как онкогенов, были результаты экспериметальных исследований, которые показали, что эти гены одновременно с воспалением, вакуолизацией цитоплазмы эукариот детерминируют предраковое изменение конструкции клеток [4 с.3; 5 с.3] и аденокарциному желудка [11 с.3]. Была показана синергичность действия генов cagA, vacA, babA2 при кишечной метаплазии [16 с.3], а присутствие в геноме бактерии гена адгезии babA2, одного или в сочетании с cagA, vacAs1 - статистически достоверно ассоциируется с развитием пренеопластических изменений в желудке пациентов [15 с.3]. Экспериментально подтверждено, что белок СagA, продукт главного гена патогенности сagA, одновременно функционирует как эпигенетический онкопротеин, провоцирующий развитие ранних фаз развития рака желудка [6 с.3]. Обнаруженная недавно новая детерминанта гена vacA - регион i1 Нelicobacter pylori более тесно чем аллели гена vacA s1m1 достоверно ассоциируется с дистальной аденокарциномой желудка [12 с.3].
Таким образом, гены патогенности оказались полифункциональными, так как детерминируют и факторы патогенности, и канцерогенез [9 с.3].
Полифукциональность онкогенов хеликобактера – новая, ранее неизвестная, особеннность генетического потенциала H. pylori. Полагают, что гены cagA, vacA, babA2 уже на стадии хронического гастрита индуцируют развитие последующих стадий: атрофического гастрита, метаплазии, дисплазии и последней стадии – аденокарциномы [11 с.4].
Особенностью бактериальных онкогенов является их уникальность. В частности, последовательности cagA не встречаются среди других видов хеликобактерий, гомолог гена сagA не обнаружен ни в одном виде бактерий вообще. Вакуолизирующий цитотоксин VacA, детерминируемый онкогеном vacA, - уникальный экзотоксин бактерий, аминокислотные последовательности которого не встречаются ни у одного из известных бактериальных или эукариотических белков. В связи с этим вряд ли можно согласиться с предположением, что cagA и vacA могли быть перенесены в H. pylori от других микроорганизмов с помощью острова патогенности или иным путем.
Онкогены H. pylori участвуют в канцерогенезе, как правило, в ассоциации. Так, онкогенные хеликобактериозы способны индуцировать только cagA+ штаммы в ассоциации с vacAs1, а babA2 при кишечной метаплазии может ассоциироваться с генами cagA, vacA.
Бактериальный онкогенез отличается от вирусного оригинальным способом передачи генетической информации в клетку-мишень. Если вирусы, используя эндоцитоз, проникают внутрь клетки вместе с вирионом и затем встраивают в геном клетки свой онкоген, то онкогены бактерии после ее адгезии на поверхности клетки только детерминируют поступление внутрь клетки онкобелка CagA и цитотоксина VacA, сохраняя, как правило, внеклеточную локализацию.
Согласно вирусо-генетической теории возникновения рака, интеграция генома или части генома вируса является обязательным и необходимым условием вирусного канцерогенеза. Отсутствие интеграции онкогенов при бактериальном канцерогенезе обуслaвливает эпигенетический его характер, когда проникающие в клетку продукты онкогенов бактерии инициируют малигнизацию, не изменяя геном клетки. Bирусные же онкогены, напротив, трансформируют клетки вследствие интеграции в их геном.
Эпигенетическое фосфорилирование, эпигеномный характер хеликобактерной малигнизации - особенность бактериального канцерогенеза. Состояние «предрака» при хеликобактерной инфекции в виде эпидермального мезенхимального превращения (ЕМТ), как заключительного этапа прогрессии эпителиальной опухоли – приобретение черт фибробластов, подтверждает эпигенетический механизм хеликобактерной малигнизации. Эти изменения имеют физиологическую природу, а не генетическую, и обратимы [1 c.4].
Внеклеточная локализация онкогенов обуславливает также неспособность хеликобактера активировать протоонкогены клетки и индуцировать инсерционный мутагенез, что может иметь место при вирусном канцерогенезе.
В отличие от небактериальных онкогенезов, когда при немелкоклеточном раке человека, саркоме Рауса кур используются только рецепторные тирозинкиназы, а при раке печени, инициированном вирусом гепатита В, -цитозольные, при бактериальном, наряду с рецепторными в фосфорилирование вовлекаются также цитозольные(нерецепторные) тирозинкиназы.
Механизм канцерогенеза Helicobacter pylori представлен на рис. 1.
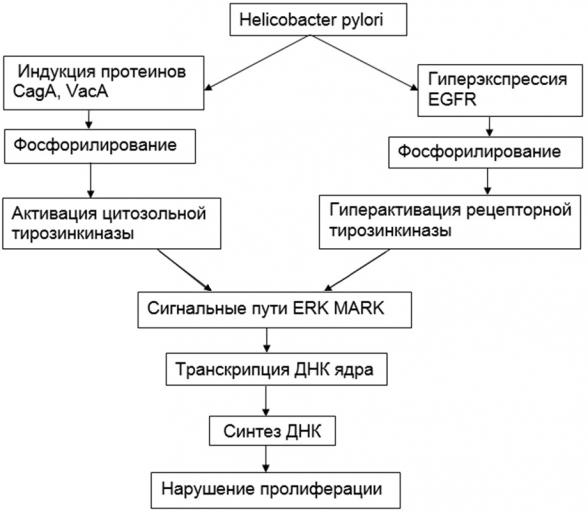
Рис.1. Механизм онкогенеза Helicobacter pylori
Итак, главным механизмом бактериального, как и вирусного онкогенного канцерогенеза, вляется тирозинкиназное фосфорилирование. В процессе фосфорилирования хеликобактер активирует рецепторные тирозинкиназы EGFR и цитозольные тирозинкиназы цитоплазмы клетки.
В дальнейшем для фосфорилирования бактерия использует общие с EGFR рецептором ERK MARK митогенные сигнальные пути, по которым сигнал передается в ядро клетки, где активируется транскрипция генов ядра, происходит синтез и репликация ДНК, что определяет начало митоза. В результате нарушается нормальный G1,S,G2 цикл митоза, стимулируется и нарушается пролиферация. Гиперпролиферация клеток считается основным признаком опухолевого роста.
Усиленная пролиферация отмечалась Yu et al. (2002) у пациентов инфицированных babA2 штаммами cagA+vacAs1 генотипов с пренеопластическими изменениями в желудке [15 с. 6].
Онкобелок СagA, продукт онкогена сagA, является первым онкобелком бактериального происхождения, вовлеченным в процесс канцерогенеза. Поступив внутрь клетки по 4 типу секреции с помощью генов острова патогенности cag PAI (около 40 генов), CagA фосфорилируется тирозиновыми протеинкиназами семейства Src клетки (детерминируются протоонкогеном с–src). Тирозинфосфорилированный белок CagA присоединяется и активирует фосфатазу SHP-2 и Sck киназу. Важную роль в активации SHP-2 фосфатазы имеет SH-2 домены, которые непосредственно является мишенью для фосфорилированного CagA. Активирование фосфатазы и киназы приводит к ненормальному активированию и запуску каскада MARK ERK киназ сигнальных путей клетки, что подобно неудержимой стимуляции EGF фактора может повышать риск развития рака желудка [4 с.6; 5 с.6;10 с.6].
Активация тирозинкиназ осуществляется с помощью SH-2 доменов. Внутриклеточный домен рецептора EGFR активируется собственными доменами SH-2 и вследствие этого приобретает тирозинкиназную активность. При фосфорилировании СagA домены SH-2 тирозинфосфатазы также аналогично активируют тирозинфосфатазы клетки
Вследствие фосфорилирования СagA нарушаются межклеточные контакты и цитоскелет клеток, полярность и подвижность, стимулируется пролиферация париетальных клеток желудка [14 с.6]. Белки семействa Src участвуют также в передаче интегринзависимых сигналов в клетке, которые побуждают ее деление.
Клетка как будто не распознает чужеродный для нее бактериальный онкобелок СagA, который фосфорилируется подобно эпидермальному фактору роста EGF - (EGF-like) при нормальном метаболизме и протекает аналогично фосфорилированию нормальных компонентов клетки.
В результате фосфорилирования СagA создается дополнительный к нормальному, автономный эффект активации тирозинкиназ клетки и пролиферация, которые не зависят от цикличной G1,S,G2 пролиферации, регулируемой в неинфицированных клетках EGFR рецептором, и, таким образом, нарушается нормальная цикличность пролиферации клеток. Поступление новых порций онкобелка СagA внутрь клетки при длительном инфицировании в различные фазы ее пролиферации может создавать также эффект стимуляции и дерегулирования пролиферации.
Следует отметить, что аналогичная автономная, нерегулируемая клеткой пролиферация при вирусном канцерогенезе, в отличие от бактериальной, детерминируется доминантными онкогенами вирусов, интегрированными в геном клетки.
С тирозинкиназным фосфорилированием SH-2 связан и «колибри фенотип» хеликобактера (удлинение клеток культуры ткани), который утрачивается при ингибировании трансферазы, разрушении комплекса фосфорилированный СagA + SHP2, отсутствии домена SH2. Этот феномен, обусловленный влиянием СagA Helicobacter pylori на цитоскелет клетки, аблюдается уже через 36 часов в опытах с культурой клеток AGS[13 c.7].
Цитотоксин VacA, также как и СagA, активирует внутриклеточные цитозольные тирозинкиназы и сигнальные пути. Активируя тирозинкиназы после проникновения внутрь клетки субъединица А VacA, тем самым дополнительно усиливает эффект активации, достигаемый фосфорилированием CagA.
Субъединица В VacA, отвечающая за адсорбцию токсина на поверхности клетки, в случае присоединения к EGFR, возможно, может играть роль лиганда и активировать вследствие этого внутриклеточный домен рецептора, который, как известно, обладает рецепторной тирозинкиназной активностью.
Гиперэкспрессия EGFR клетки, обнаруженная при инфицировании вирулентными хеликобактерами, приводит к изменению трансдукции, гиперэкспрессии сигнальных путей, изменению профиля активации генов [8 с.7]. При этом сохраняется тирозинкиназный механизм фосфорилирования внутриклеточного домена, что приводит к трансактивации рецепторной тирозинкиназы.
Таким образом, фосфорилирование EGFR рецептора и продуктов онкогенов при онкогенном хеликобактериозе дает суммарный эффект избыточной гиперактивации тирозинкиназ, что и является ключевым механизмом бактериального онкогенеза, в результате которого нарушается пролиферация.
Известно, что активация тирозинкиназ, имеет место также при некоторых других небактериальных канцерогенезах. При гепатобилиарной карциноме (вирус гепатита В), например, активируются тирозинкиназы семейства Src, а при гиперактивации тирозинкиназы внутриклеточного домена EGFR, когда последний работает в режиме постоянной активации, - возникает немелкоклеточный рак легкого.
Следует отметить, что одинаковый тирозинкиназный путь сохраняется в случае несколько отличных молекулярных механизмах малигнизации при вирусном канцерогенезе животных и бактериальном у человека. Так, при саркоме Рауса трансформация клеток ассоциируется с неудержимой продукцией избыточной тирозинкиназы вируса – аналога рецепторной тирозинкиназы клетки. Создается эффект дозы онкогена.
При бактериальном канцерогенезе вместо избыточной продукции имеет место избыточная активация тирозинкиназ. Обращает на себя внимание, что тирозинкиназы обнаружены в нормальных эпителиальных клетках человека и животных и активация тирозинкиназы внутриклеточного домена имеет место при нормальном метаболизме клеток. Малигнизацию клеток индуцирует избыточная продукция и избыточная активация тирозинкиназ, и, следовательно, количественные, а не качественные изменения лежат в основе как вирусного так и бактериального онкогенеза.
Хронический хеликобактерный канцерогенез в процессе длительного инфицирования может приводить к нарушению митоза и пролиферации клеток. В настоящее время то, что «хронический митогенез ведет к мутагенезу» рассматривается как универсальный механизм онкогенеза [12 с.8].
Можно предположить, что при длительной, в течение десятилетий, инфицированности хеликобактером, вследствие накопления в геноме клетки инфицированных людей спонтанных и индуцированных мутаций, возможна трансформация эпигенетического пути канцерогенеза в генетический.
Считается, что при отсутствии лечения однажды инфицированный человек может сохранять хеликобактер в организме пожизненно. Риск развития онкогенного заболевания, прежде всего, зависит от генетического потенциала шамма бактерии. Дистальная аденокарцинома желудка и MALT лимфома ассоциируются с присутствием в геноме бактерии гена cagA (cagA+ штаммы), онкогенов cagA, vacA, babA2, наличием у vacA гена s1m1 аллелей и региона i1.
1. Абелев Г.И., Эрайзер Г.Л. На пути к пониманию природы рака\\ Биохимия.-2008.-73.-5.-С. 605-618.
2. Чернявский В.Н.,Бирюкова С.В.,Мартынов А.В. и др. Helicobacter pylori- Herpesvsridae ассоциации в этиопатогенезе поражения желудка, современные аспекты изучения.\\Анали Мечніковського інституту.-2005.-1.- С. 48-65.
3. Hatakeyama M. The role of Helicobacter pylori CagA in gastric carcinogenesis //Int.J.Hemat.-2006.-84(4).- P.301-308.
4. Hatakeyama M. Helicobacter pylori and cancerogenesis//J. Gastroenterol.-2009.-44(4).-P.239-248.
5. Higashi H., Tsutsumi R., Muto S. et al. SHP-2 Tyrosine Phosphatase as an Intracellular Target of Helicobacter pylori CagA Protein//Science.-2002.-295.-P.683-686.
6. Ishikawa S.,Ohta T., Hatakeyama M. Stability of Helicobacter pylori CagA oncoprotein sn human gastric epithelial cells//FEBS letters.-2009.- 583(14)/- P.2414-2418.
7. Kew M.C.//Hepatitis B virus X protein in the pathogenesis of hepatitis B virus-induced hepatocelulae carcinoma//J.Gastroenterol.Hepatol.-2011.-26.-Suppl.1-P.144-152.
8. Кim J.,Kim N., Park J.H. et al.//The Effect of Helicobacter pylori on Growth Factor Receptor-induced Signal Transduction and the Preventive Effect of Celecoxib in Gastric Cancer Cells.- Gut. Liver.-2013.-7(5).- P.552-559.
9. Кованова Е.М., Климнюк С.І., Творко М.С. Гени cаgA,vacA Helicobacter pylori, асоційовані з раком шлунка\\ Збірник матеріалів міжнародної науково-практичної конференції «Медична наука та практика ХХ1 століття».-Київ.- 2012.-С.12-15.
10. Peek K.M.Jr., Blaser M.J., Mays D.J. et al. Helicobacter pylori strain – specific genotypes and modulation of the gastric epithelial cell cycle// Cancer Res.- 1999.-15.-59(24).-P. 6124.-6131.
11. Leung W.K. Helicobacter pylori and Gastric Neoplasma//Infection and Inflammation: Impact on Oncogenesis.Contribution to Microbiologiy.-2006.- 13.-P.66-80.
12. Rhead J.L., Letley D.P., Mohamandi M. et al. A new determinante vaculating cytotoxin Helicobacter pylori – intermediated region is associated with gastric cancer// Gastroenterology.- 2007.-133.-3.- P.926-936.
13. Segal E.D., Cha J., Lo J. et al. Altered states:Involvement of phosphorilated CagA in the induction of host cellular growth changes by Helicobacter pylori//Proc. NatI. Acad. Sci. USA.-1999.- 7.-96(25).- P.14559-14564.
14. Yokota S., Okabayashi T., Rehli M. et al.//Helicobacter pylori lipopolisacharides upregulate toll-live receptor 4 expression and proliferation of gastric epithelial cells via the MEK ½ -Erk1/2 mitogen-activated protein-kinase pathway//Infect. Immun. -2010.-76.-1.-P.468-476.
15. Yu J., Leung W.K.,Go M.Y. et al. Relationship between Helicobacter pylori babA2 status with gastric epithelial turnover and prevalignant gastric lesions. //Gut.- 2002.-51.-P.480-484.
16. Zumbon C.F.,Novaglia F., Basso D. et al. Helicobacter pylori babA2, cagA, and s1 vacA genes work sinergistically in cousing intestinal metaplasia//J.Clin.Path. – 2003.-56.- P. 287-296.
Рецензии:
21.06.2014, 22:03 Лахтин Юрий Владимирович
Рецензия: Представленный авторами подробный обзор прокариот-генетического механизма онкогенеза H.pylori актуален, интересен и полезен для специалистов. Рекомендуется к публикации.
Уважаемый Юрий Владимирович! Благодарим Вас за положительную оценку и рекомендацию к печати нашей статьи "Прокариот-генетическая эпигенетическая теория......"
16.07.2014, 17:15 Остапенко Ольга Валериевна
Рецензия: Статья "ПРОКАРИОТ-ГЕНЕТИЧЕСКАЯ ЭПИГЕНЕTИЧЕСКАЯ ТЕОРИЯ КАНЦЕРОГЕНЕЗА, АССОЦИИРОВАННОГО С HELICOBACTER PYLORI" Ковановой Э.Н. написана на высоком научном уровне. Рекомендую к печати.
Комментарии пользователей:
Оставить комментарий
Вверх